Dandanes je nealkoholna zamaščenost jeter (NAFLD) postala glavni vzrok kronične bolezni jeter na Kitajskem in celo po svetu. Spekter bolezni vključuje preprost jetrni steatohepatitis, nealkoholni steatohepatitis (NASH) ter z njim povezano cirozo in raka jeter. Za NASH je značilno prekomerno kopičenje maščobe v hepatocitih in povzročena celična poškodba ter vnetje, z jetrno fibrozo ali brez nje. Resnost jetrne fibroze pri bolnikih z NASH je tesno povezana s slabo prognozo za jetra (ciroza in njeni zapleti ter hepatocelularni karcinom), srčno-žilnimi dogodki, zunajjetrnimi malignimi obolenji in smrtjo zaradi vseh vzrokov. NASH lahko negativno vpliva na kakovost življenja bolnikov; vendar za zdravljenje NASH še ni bilo odobrenih nobenih zdravil ali terapij.
Nedavna študija (ENLIVEN), objavljena v New England Journal of Medicine (NEJM), je pokazala, da je pegozafermin izboljšal tako jetrno fibrozo kot vnetje jeter pri bolnikih z biopsijo brez ciroze.
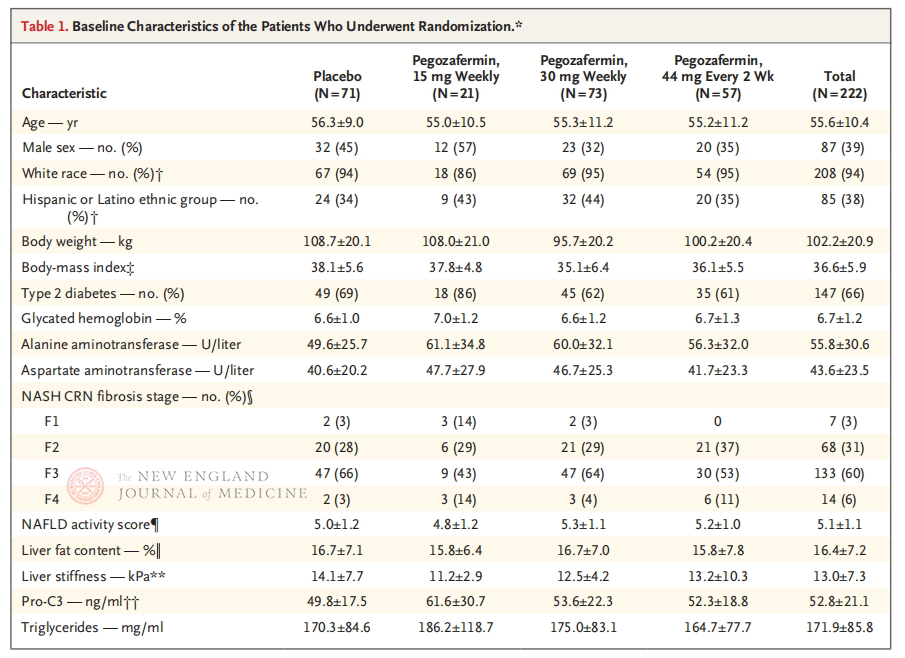
V multicentrično, randomizirano, dvojno slepo, s placebom nadzorovano klinično preskušanje faze 2b, ki ga je izvedel profesor Rohit Loomba s svojo klinično ekipo na Medicinski fakulteti Univerze v Kaliforniji v San Diegu, je bilo med 28. septembrom 2021 in 15. avgustom 2022 vključenih 222 bolnikov z z biopsijo potrjenim NASH stadija F2-3. Bolniki so bili naključno razporejeni v skupino, ki je prejemala pegozafermin (subkutana injekcija, 15 mg ali 30 mg enkrat na teden ali 44 mg enkrat na 2 tedna) ali placebo (enkrat na teden ali enkrat na 2 tedna). Primarni opazovani dogodki so vključevali izboljšanje fibroze ≥ 1. stopnje in odsotnost napredovanja NASH. NASH se je izzvenel brez napredovanja fibroze. V študiji je bila opravljena tudi ocena varnosti.
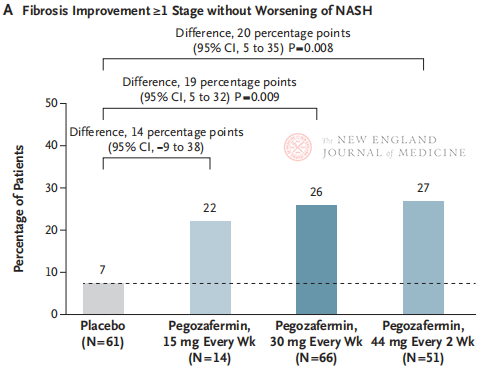
Po 24 tednih zdravljenja je bil delež bolnikov z izboljšanjem fibroze ≥ 1. stopnje in brez poslabšanja NASH ter delež bolnikov z regresijo NASH in brez poslabšanja fibroze bistveno večji v treh skupinah z odmerki pegozafermina kot v skupini s placebom, z večjimi razlikami pri bolnikih, zdravljenih s 44 mg enkrat na dva tedna ali 30 mg enkrat na teden. Kar zadeva varnost, je bil pegozafermin podoben placebu. Najpogostejši neželeni učinki, povezani z zdravljenjem s pegozaferminom, so bili slabost, driska in eritem na mestu injiciranja. V tej študiji faze 2b predhodni rezultati kažejo, da zdravljenje s pegozaferminom izboljša jetrno fibrozo.
Pegozafermin, uporabljen v tej študiji, je dolgodelujoči glikoliran analog humanega fibroblastnega rastnega faktorja 21 (FGF21). FGF21 je endogeni presnovni hormon, ki ga izločajo jetra in ima vlogo pri uravnavanju presnove lipidov in glukoze. Prejšnje študije so pokazale, da ima FGF21 terapevtske učinke na bolnike z NASH s povečanjem občutljivosti jeter na inzulin, spodbujanjem oksidacije maščobnih kislin in zaviranjem lipogeneze. Vendar pa kratek razpolovni čas naravnega FGF21 (približno 2 uri) omejuje njegovo uporabo pri kliničnem zdravljenju NASH. Pegozafermin uporablja tehnologijo glikozilirane pegilacije za podaljšanje razpolovnega časa naravnega FGF21 in optimizacijo njegove biološke aktivnosti.
Poleg pozitivnih rezultatov v tej klinični študiji faze 2b je še ena nedavna študija, objavljena v reviji Nature Medicine (ENTRIGUE), pokazala, da pegozafermin pri bolnikih s hudo hipertrigliceridemijo znatno zniža tudi trigliceride, ne-HDL holesterol, apolipoprotein B in jetrno steatozo, kar lahko pozitivno vpliva na zmanjšanje tveganja za srčno-žilne dogodke pri bolnikih z NASH.
Te študije kažejo, da lahko pegozafermin kot endogeni presnovni hormon bolnikom z NASH zagotovi številne presnovne koristi, zlasti ker se lahko NASH v prihodnosti preimenuje v presnovno povezano zamaščenost jeter. Zaradi teh rezultatov je zelo pomembno potencialno zdravilo za zdravljenje NASH. Hkrati bodo ti pozitivni rezultati študije podprli vključitev pegozafermina v klinična preskušanja 3. faze.
Čeprav je tako dvotedensko zdravljenje s 44 mg pegozafermina kot tedensko zdravljenje s 30 mg pegozafermina doseglo histološki primarni cilj preskušanja, je bilo zdravljenje v tej študiji trajanje le 24 tednov, stopnja upoštevanja navodil v skupini s placebom pa le 7 %, kar je bistveno nižje od rezultatov prejšnjih kliničnih študij, ki so trajale 48 tednov. Ali so razlike in varnost enake? Glede na heterogenost NASH so v prihodnosti potrebna večja, večcentrična, mednarodna klinična preskušanja, ki bodo vključevala večje populacije bolnikov in podaljšala trajanje zdravljenja, da bi bolje ocenili učinkovitost in varnost zdravila.
Čas objave: 16. september 2023