Kaheksija je sistemska bolezen, za katero so značilni izguba teže, atrofija mišičnega in maščobnega tkiva ter sistemsko vnetje. Kaheksija je eden glavnih zapletov in vzrokov smrti pri bolnikih z rakom. Ocenjuje se, da lahko incidenca kaheksije pri bolnikih z rakom doseže od 25 % do 70 %, vsako leto pa po vsem svetu trpi zaradi kaheksije približno 9 milijonov ljudi, od katerih jih 80 % umre v enem letu po diagnozi. Poleg tega kaheksija pomembno vpliva na kakovost življenja bolnikov in poslabša toksičnost, povezano z zdravljenjem.
Učinkovito posredovanje pri kaheksiji je zelo pomembno za izboljšanje kakovosti življenja in prognoze bolnikov z rakom. Vendar pa so kljub določenemu napredku pri preučevanju patofizioloških mehanizmov kaheksije mnoga zdravila, razvita na podlagi možnih mehanizmov, le delno učinkovita ali neučinkovita. Trenutno ni učinkovitega zdravljenja, ki bi ga odobrila ameriška Uprava za hrano in zdravila (FDA).
Kaheksija (sindrom hiranja) je zelo pogosta pri bolnikih z mnogimi vrstami raka, kar pogosto povzroči izgubo teže, atrofijo mišic, zmanjšano kakovost življenja, okvarjeno delovanje in skrajšano preživetje. V skladu z mednarodno dogovorjenimi standardi je ta večfaktorski sindrom opredeljen kot indeks telesne mase (ITM, teža [kg], deljena s kvadratom višine [m]), manjši od 20 ali, pri bolnikih s sarkopenijo, izguba teže za več kot 5 % v šestih mesecih ali izguba teže za več kot 2 %. Trenutno v Združenih državah Amerike in Evropi ni odobrenih nobenih zdravil posebej za zdravljenje rakave kaheksije, kar ima za posledico omejene možnosti zdravljenja.
Nedavne smernice, ki priporočajo nizke odmerke olanzapina za izboljšanje apetita in telesne teže pri bolnikih z napredovalim rakom, v veliki meri temeljijo na rezultatih študije v enem samem centru. Poleg tega lahko kratkotrajna uporaba analogov progesterona ali glukokortikoidov prinese omejene koristi, vendar obstaja tveganje za neželene stranske učinke (kot je uporaba progesterona, povezana s trombemboličnimi dogodki). Klinična preskušanja drugih zdravil niso pokazala zadostne učinkovitosti za pridobitev regulativne odobritve. Čeprav je bil anamorin (peroralna različica peptidov, ki sproščajo rastni hormon) na Japonskem odobren za zdravljenje rakave kaheksije, je zdravilo le do določene mere povečalo telesno sestavo, ni izboljšalo moči oprijema in ga ameriška Uprava za hrano in zdravila (FDA) na koncu ni odobrila. Nujno so potrebna varna, učinkovita in ciljno usmerjena zdravljenja rakave kaheksije.
Faktor rastne diferenciacije 15 (GDF-15) je citokin, ki ga povzroča stres in se veže na protein, podoben receptorju alfa, iz družine nevrotrofičnih faktorjev, ki izvira iz glije, v zadnjem delu možganov. Pot GDF-15-GFRAL je bila opredeljena kot glavni regulator anoreksije in uravnavanja telesne teže ter igra vlogo pri patogenezi kaheksije. V živalskih modelih lahko GDF-15 povzroči kaheksijo, zaviranje GDF-15 pa lahko ublaži ta simptom. Poleg tega so povišane ravni GDF-15 pri bolnikih z rakom povezane z zmanjšano telesno težo in maso skeletnih mišic, zmanjšano močjo in skrajšanim preživetjem, kar poudarja vrednost GDF-15 kot potencialne terapevtske tarče.
Ponsegromab (PF-06946860) je visoko selektivno humanizirano monoklonsko protitelo, ki se lahko veže na GDF-15 v krvnem obtoku in s tem zavira njegovo interakcijo z receptorjem GFRAL. V majhni odprti študiji faze 1b je bilo 10 bolnikov z rakavo kaheksijo in povišanimi ravnmi GDF-15 v krvnem obtoku zdravljenih s ponsegromabom, pri čemer so se jim izboljšale telesna teža, apetit in telesna aktivnost, medtem ko so bile ravni GDF-15 v serumu zavrte, neželeni učinki pa nizki. Na podlagi tega smo izvedli klinično preskušanje faze 2 za oceno varnosti in učinkovitosti ponsegromaba pri bolnikih z rakavo kaheksijo in povišanimi ravnmi GDF-15 v krvnem obtoku v primerjavi s placebom, da bi preizkusili hipotezo, da je GDF-15 primarni patogenetični dejavnik bolezni.
V študijo so bili vključeni odrasli bolniki s kaheksijo, povezano z rakom (nedrobnocelični pljučni rak, rak trebušne slinavke ali kolorektalni rak), s serumsko ravnjo GDF-15 vsaj 1500 pg/ml, oceno stanja telesne pripravljenosti po lestvici Eastern Tumor Consortium (ECOG) ≤ 3 in pričakovano življenjsko dobo vsaj 4 mesece.
Vključeni bolniki so bili naključno dodeljeni v skupino, ki je subkutano prejemala 3 odmerke ponsegromaba 100 mg, 200 mg ali 400 mg ali placeba, vsake 4 tedne v razmerju 1:1:1. Primarni opazovani dogodek je bila sprememba telesne teže glede na izhodišče po 12 tednih. Ključni sekundarni opazovani dogodek je bila sprememba od izhodišča v rezultatu podlestvice anoreksijske kaheksije (FAACT-ACS), ki ocenjuje terapevtsko delovanje pri anoreksijski kaheksiji. Drugi sekundarni opazovani dogodki so vključevali rezultate dnevnika simptomov kaheksije, povezane z rakom, izhodiščne spremembe telesne dejavnosti in opazovane dogodke hoje, izmerjene z nosljivimi digitalnimi zdravstvenimi napravami. Zahteve glede minimalnega časa nošenja so določene vnaprej. Ocena varnosti je vključevala število neželenih učinkov med zdravljenjem, rezultate laboratorijskih testov, vitalne znake in elektrokardiograme. Eksplorativni opazovani dogodki so vključevali izhodiščne spremembe indeksa ledvenih skeletnih mišic (površina skeletnih mišic, deljena s kvadratom višine), povezanega s sistemskimi skeletnimi mišicami.
Skupno 187 bolnikov je bilo naključno razporejenih v skupino, ki je prejemala ponsegromab 100 mg (46 bolnikov), 200 mg (46 bolnikov), 400 mg (50 bolnikov) ali placebo (45 bolnikov). Štiriinsedemdeset (40 odstotkov) jih je imelo nedrobnocelični pljučni rak, 59 (32 odstotkov) raka trebušne slinavke in 54 (29 odstotkov) kolorektalnega raka.
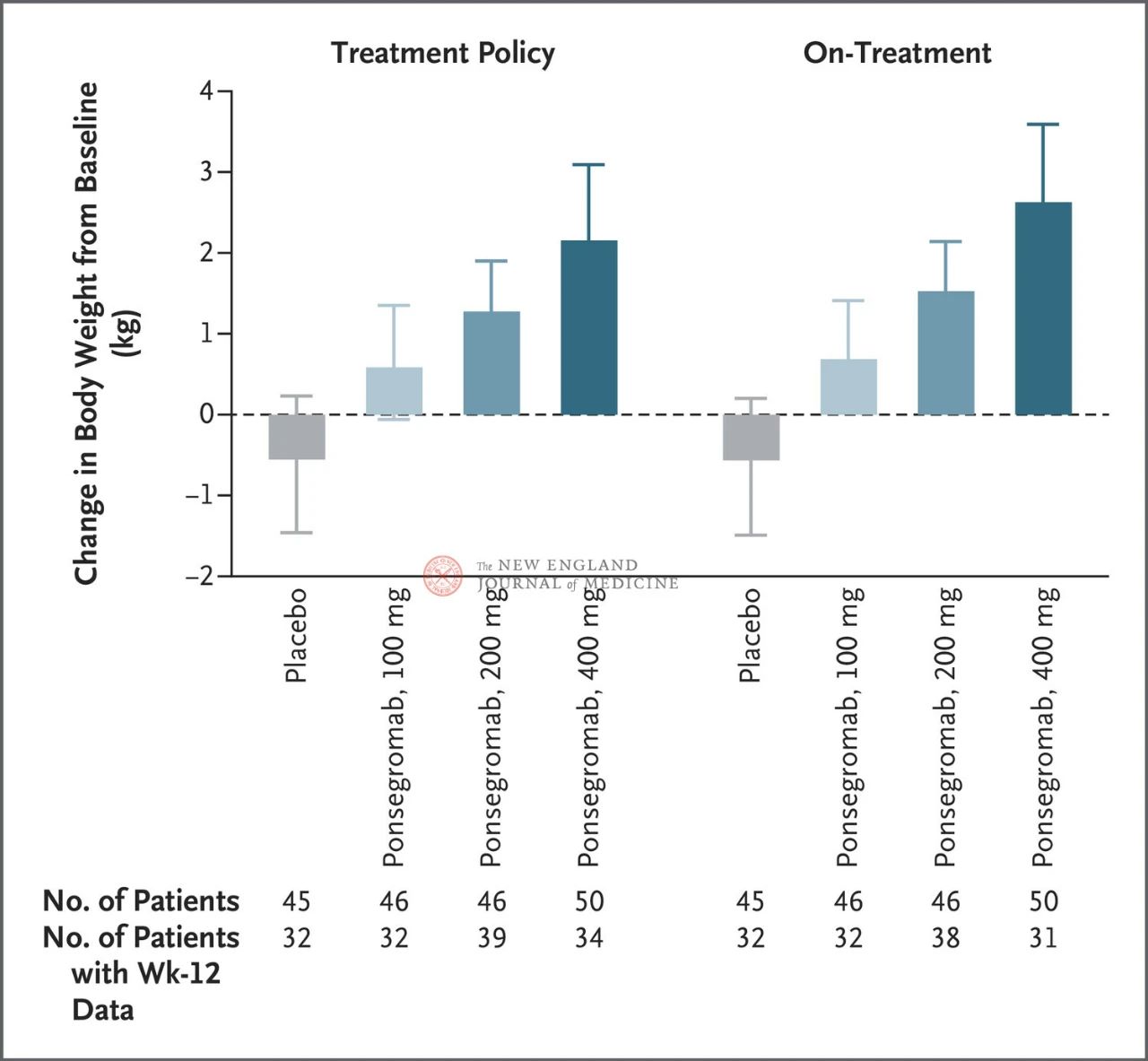
Razlike med skupinami s 100 mg, 200 mg in 400 mg ter placebom so bile 1,22 kg, 1,92 kg oziroma 2,81 kg.
Slika prikazuje primarni opazovani dogodek (sprememba telesne teže od izhodišča do 12. tedna) pri bolnikih z rakavo kaheksijo v skupinah, ki so prejemale ponsegromab, in skupini s placebom. Po prilagoditvi za konkurenčno tveganje smrti in druge sočasne dogodke, kot je prekinitev zdravljenja, je bil primarni opazovani dogodek analiziran s stratificiranim modelom Emax z uporabo rezultatov Bayesove skupne longitudinalne analize iz 12. tedna (levo). Primarni opazovani dogodki so bili analizirani tudi na podoben način z uporabo ocenjenih ciljev za dejansko zdravljenje, kjer so bila opažanja po vseh sočasnih dogodkih skrajšana (desna slika). Intervali zaupanja (navedeni v članku
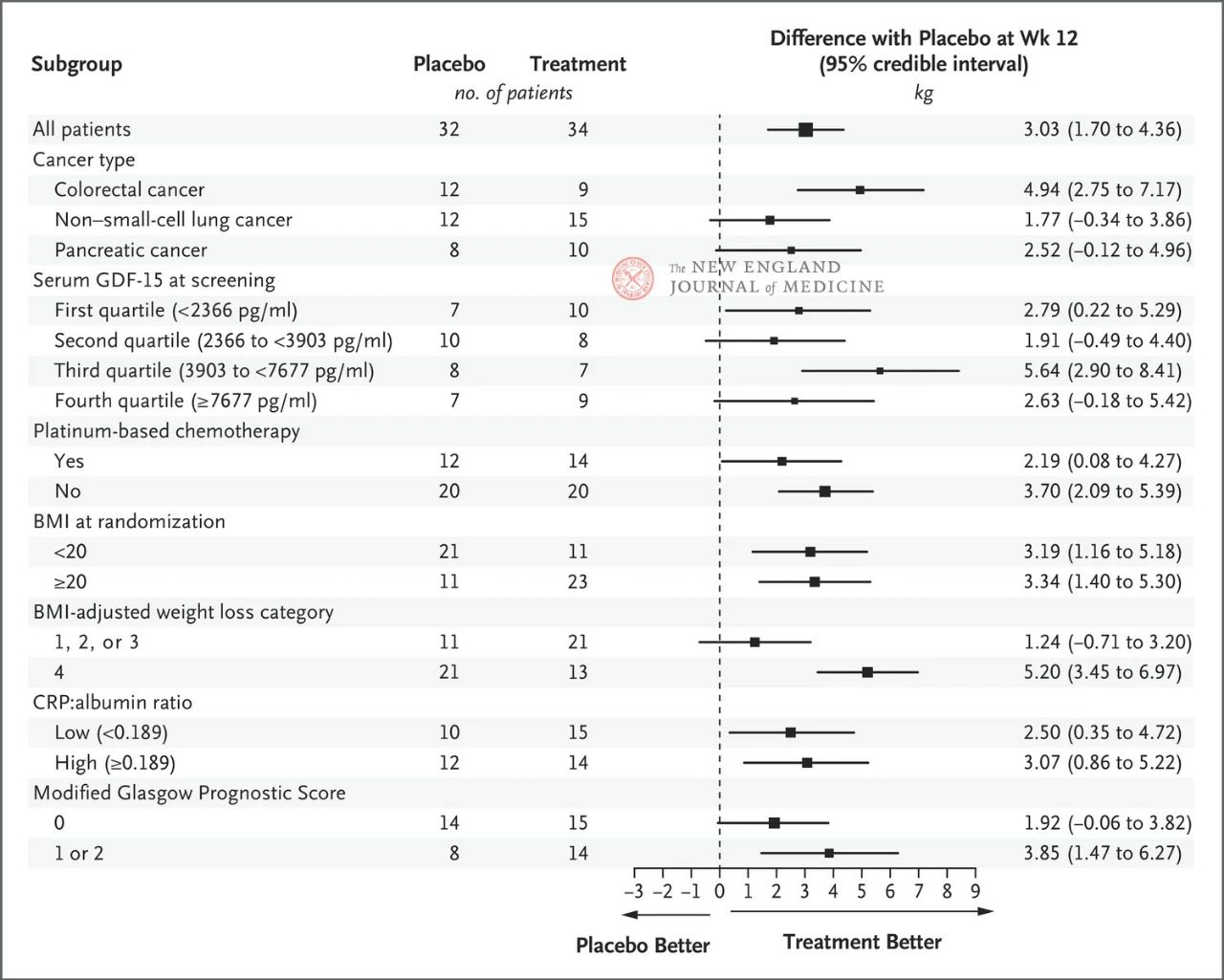
Učinek 400 mg ponsegromaba na telesno težo je bil dosleden v vseh glavnih vnaprej določenih podskupinah, vključno z vrsto raka, kvartilom serumske ravni GDF-15, izpostavljenostjo kemoterapiji na osnovi platine, ITM in izhodiščnim sistemskim vnetjem. Sprememba teže je bila skladna z zaviranjem GDF-15 po 12 tednih.
Izbor ključnih podskupin je temeljil na post-hoc Bayesovi skupni longitudinalni analizi, ki je bila izvedena po prilagoditvi za kompetitivno tveganje smrti na podlagi ocenjenega cilja strategije zdravljenja. Intervali zaupanja se ne smejo uporabljati kot nadomestilo za testiranje hipotez brez večkratnih prilagoditev. ITM predstavlja indeks telesne mase, CRP predstavlja C-reaktivni protein in GDF-15 predstavlja faktor rastne diferenciacije 15.
Na začetku je večji delež bolnikov v skupini, ki je prejemala ponsegromab 200 mg, poročal o odsotnosti zmanjšanja apetita; v primerjavi s placebom so bolniki v skupinah, ki so prejemali ponsegromab 100 mg in 400 mg, poročali o izboljšanju apetita od izhodišča po 12 tednih, s povečanjem rezultatov FAACT-ACS za 4,12 oziroma 4,5077. Med skupino, ki je prejemala 200 mg, in skupino, ki je prejemala placebo, ni bilo pomembne razlike v rezultatih FAACT-ACS.
Zaradi vnaprej določenih zahtev glede časa nošenja in težav z napravo je 59 oziroma 68 bolnikov posredovalo podatke o spremembah telesne aktivnosti in končnih točk hoje glede na izhodišče. Med temi bolniki so bolniki v skupini s 400 mg v primerjavi s skupino, ki je prejemala placebo, po 12 tednih zabeležili povečanje splošne aktivnosti, in sicer 72 minut nesedeče telesne aktivnosti na dan. Poleg tega se je v skupini s 400 mg po 12 tednih povečal tudi indeks ledvenih skeletnih mišic.
Incidenca neželenih učinkov je bila v skupini, ki je prejemala ponsegromab, 70 % v primerjavi z 80 % v skupini, ki je prejemala placebo, in so se pojavili pri 90 % bolnikov, ki so sočasno prejemali sistemsko zdravljenje proti raku. Incidenca slabosti in bruhanja je bila v skupini, ki je prejemala ponsegromab, manjša.
Čas objave: 05. oktober 2024